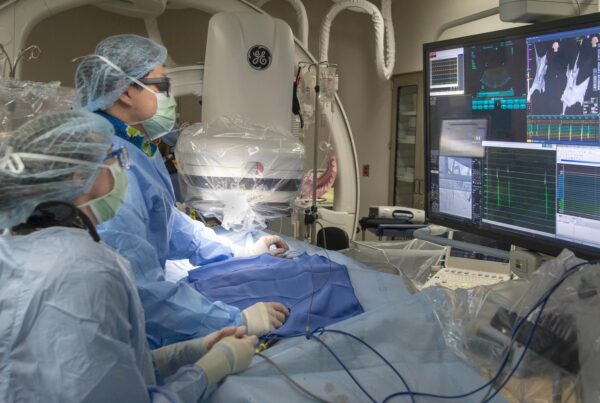
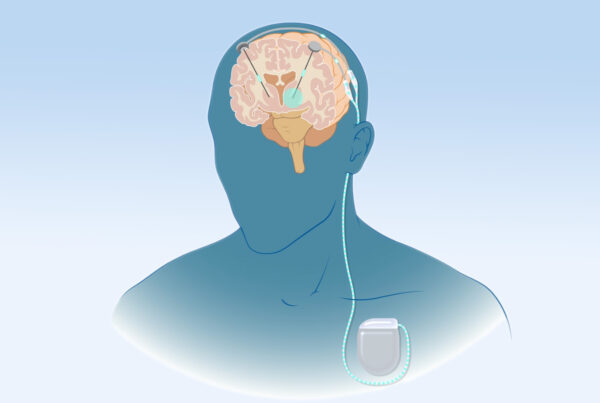
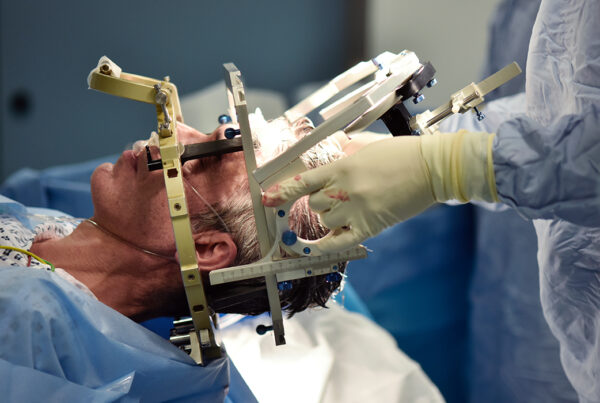
في رحلتنا المستمرة نحو فهم الأمراض المعقدة ومكافحتها، برز العلاج الأحادي النسيلة (Monoclonal Antibody Therapy) كأحد أبرز الابتكارات التي أعادت تشكيل مشهد الطب الحديث.
لسنوات طويلة، كانت العلاجات تعتمد غالبًا على نهج عام، يستهدف الخلايا بشكل واسع، مما قد يؤثر على الأنسجة السليمة إلى جانب المريضة.
لكن العلاج الأحادي النسيلة قدم مفهومًا جديدًا: الدقة المتناهية.
إنه أشبه بتصميم مفاتيح فريدة تتناسب مع أقفال محددة على الخلايا المريضة، مما يسمح باستهداف دقيق وفعال، ويقلل من الأضرار الجانبية.
هذه الأجسام المضادة المصممة في المختبر ليست مجرد أدوية، بل هي أدوات بيولوجية ذكية، قادرة على التعرف على جزيئات معينة بدقة فائقة.
يمثل العلاج الأحادي النسيلة بارقة أمل للملايين حول العالم، ويفتح آفاقًا واسعة لعلاج أمراض كانت تُعتبر مستعصية في السابق.
يمثل العلاج الأحادي النسيلة ثورة حقيقية في الطب الدقيق. بتطوره المستمر وبتطبيقه في مستشفى ليفا وغيرها من المؤسسات العالمية، أصبح نقطة تحول في علاج السرطان، الأمراض المناعية، وحتى الفيروسات.

فهم الأجسام المضادة
لفهم العلاج الأحادي النسيلة، يجب أن نبدأ بفهم الدور الحيوي للأجسام المضادة الطبيعية في أجسامنا.
الأجسام المضادة (Antibodies) هي بروتينات متخصصة ينتجها الجهاز المناعي استجابة لوجود مواد غريبة وضارة، تُعرف باسم المستضدات (Antigens) .
هذه المستضدات يمكن أن تكون بروتينات على سطح البكتيريا والفيروسات، أو خلايا سرطانية، أو حتى مواد مثيرة للحساسية.
كل جسم مضاد مصمم بشكل فريد للارتباط بمستضد واحد محدد، تمامًا كالقفل والمفتاح.
عند الارتباط بالمستضد، تقوم الأجسام المضادة بتحييد المادة الضارة مباشرة، أو تميزها لتسهيل تدميرها بواسطة خلايا مناعية أخرى، أو تحفز استجابة مناعية شاملة.
في الجسم البشري، تنتج الخلايا البائية (B-cells) عددًا لا يحصى من الأجسام المضادة المتنوعة، كل منها يستهدف مستضدًا مختلفًا.
لكن في العلاج الأحادي النسيلة، يستخدم العلماء تقنيات متطورة لإنتاج كميات كبيرة من نوع واحد فقط من الأجسام المضادة، التي تستهدف مستضدًا محددًا بدقة متناهية.
هذا يسمح بتركيز العلاج على الهدف المرضي دون التأثير على الخلايا السليمة بشكل واسع، محاكيًا بذلك دقة الجهاز المناعي الطبيعي ولكن مع توجيه وتحكم غير مسبوقين.
تصنيع الأجسام المضادة أحادية النسيلة
يُعد تصنيع الأجسام المضادة أحادية النسيلة إنجازًا مذهلاً في الهندسة البيولوجية، يعتمد على تقنيات معقدة لإنتاج كميات كبيرة من جسم مضاد واحد متطابق جينيًا.
تبدأ العملية، التي طورها جورج كوهلر وسيزار ميلشتاين في السبعينيات وحصلا عليها على جائزة نوبل، بتحصين حيوان (عادة فأر) بالمستضد المحدد الذي يرغب العلماء في استهدافه.
يستجيب الجهاز المناعي للفأر بإنتاج خلايا بائية (B-cells) تنتج أجسامًا مضادة لهذا المستضد. بعد ذلك، يتم عزل هذه الخلايا البائية من طحال الفأر.
المشكلة أن الخلايا البائية لا يمكنها النمو والانقسام في المختبر لفترة طويلة. وللتغلب على ذلك، تُدمج هذه الخلايا البائية مع خلايا سرطانية تُعرف باسم “خلايا الورم النقوي (Myeloma Cells)” التي تتميز بقدرتها على التكاثر اللانهائي.
ينتج عن هذا الاندماج خلايا هجينة تُسمى “الخلايا الهجينة (Hybridomas)”. هذه الخلايا الهجينة تمتلك خصائص كلا الخليتين الأميتين: فهي تنتج الجسم المضاد المطلوب (من الخلية البائية) ولديها القدرة على الانقسام والتكاثر إلى ما لا نهاية في بيئة المختبر (من خلية الورم النقوي).
بعد ذلك، يتم فحص الخلايا الهجينة لاختيار النسيلة (Clone) الواحدة التي تنتج الجسم المضاد المطلوب بأعلى جودة وكمية.
تُزرع هذه النسيلة المنتخبة في مزارع خلوية ضخمة لإنتاج كميات كبيرة من الأجسام المضادة أحادية النسيلة، والتي تُنقَّى وتُعدَّل لتصبح مناسبة للاستخدام البشري، لتقليل التفاعلات المناعية ضدها .
آليات عمل العلاج الأحادي النسيلة
لا تعمل الأجسام المضادة أحادية النسيلة بآلية واحدة، بل يمكنها استخدام طرق متعددة ومختلفة لمكافحة الأمراض، اعتمادًا على المستضد الذي تستهدفه. هذه الآليات تجعلها أدوات علاجية مرنة وقوية:
- الحجب والتثبيط المباشر (Direct Blocking and Inhibition): ترتبط بعض الأجسام المضادة أحادية النسيلة بمستقبلات معينة على سطح الخلايا المريضة، مثل مستقبلات النمو. عند الارتباط، تمنع هذه الأجسام المضادة المستضد من إرسال إشارات النمو، مما يؤدي إلى وقف تكاثر الخلايا المريضة أو تحفيز موتها. مثال على ذلك هو تراستوزوماب (Herceptin) الذي يحجب مستقبل HER2 في بعض أنواع سرطان الثدي.
- تحفيز الجهاز المناعي (Immune System Activation): يمكن للأجسام المضادة أحادية النسيلة أن تعمل كـ “علامة” للخلايا المريضة، مما يسهل على الخلايا المناعية الأخرى في الجسم (مثل الخلايا القاتلة الطبيعية، والخلايا البلاعمية) التعرف عليها وتدميرها. هذا يشمل آليات مثل السمية الخلوية المعتمدة على الأجسام المضادة (ADCC) والبلعمة المعتمدة على الأجسام المضادة (ADCP).
- توصيل الأدوية السامة (Drug Delivery): تُستخدم بعض الأجسام المضادة أحادية النسيلة كـ “صواريخ موجهة” تحمل مواد سامة (مثل العلاج الكيميائي أو السموم الإشعاعية) مباشرة إلى الخلايا المريضة التي تحمل المستضد المستهدف. هذا يقلل من تعرض الخلايا السليمة للدواء السام ويقلل من الآثار الجانبية الجهازية. تُعرف هذه العلاجات بـ “المتقارنات الدوائية للأجسام المضادة (Antibody-Drug Conjugates – ADCs)”.
- تعديل الاستجابة المناعية (Immune Checkpoint Modulation): بعض الأجسام المضادة أحادية النسيلة تستهدف نقاط التفتيش المناعية (مثل PD-1 أو CTLA-4) لتحرير الجهاز المناعي من كبح الخلايا السرطانية. هذه هي أساس العلاج المناعي الحديث الذي يعزز قدرة الجسم على مهاجمة السرطان.
- تحييد الجزيئات المسببة للأمراض (Neutralizing Pathogens): في الأمراض المعدية، يمكن للأجسام المضادة أن ترتبط مباشرة بالفيروسات أو البكتيريا، وتمنعها من إصابة الخلايا أو تحييد سمومها.
تطبيقات العلاج الأحادي النسيلة
لقد أحدث العلاج الأحادي النسيلة ثورة في علاج مجموعة واسعة من الأمراض، وفتح آفاقًا لم تكن متوقعة في السابق.
أبرز هذه التطبيقات هي في مجال علاج السرطان.
تُستخدم الأجسام المضادة أحادية النسيلة لاستهداف بروتينات معينة على سطح الخلايا السرطانية، مثل HER2 في سرطان الثدي، أو EGFR في سرطان القولون والرئة، أو CD20 في سرطان الغدد الليمفاوية.
لقد أدت هذه العلاجات إلى تحسين كبير في معدلات البقاء على قيد الحياة وجودة الحياة للعديد من مرضى السرطان.
بالإضافة إلى السرطان، تلعب الأجسام المضادة أحادية النسيلة دورًا حاسمًا في علاج أمراض المناعة الذاتية والالتهابية.
في هذه الأمراض، يهاجم الجهاز المناعي أنسجة الجسم السليمة عن طريق الخطأ. تستهدف الأجسام المضادة بروتينات أو مسارات محددة تساهم في الالتهاب وتلف الأنسجة. أمثلة على ذلك تشمل علاج:
- التهاب المفاصل الروماتويدي: تستهدف الأجسام المضادة مثل إنفليكسيماب (Infliximab) أو أداليموماب (Adalimumab) عامل نخر الورم ألفا (TNF-alpha).
- الصدفية والتهاب المفاصل الصدفي: تستهدف أجسام مضادة مثل أستيكينوماب (Ustekinumab) الإنترلوكين-12/23.
- مرض كرون والتهاب القولون التقرحي: تستخدم أيضًا مثبطات TNF-alpha.
- التصلب المتعدد: بعض الأجسام المضادة تعمل على تعديل الاستجابة المناعية لتقليل هجمات المرض.
فوائد العلاج الأحادي النسيلة
يقدم العلاج الأحادي النسيلة مجموعة من الفوائد الملموسة التي تميزه عن العديد من العلاجات التقليدية، مما يجعله خيارًا مفضلاً في العديد من الحالات.
أولًا، الدقة والاستهدافية العالية: تُعد هذه الميزة الأبرز، حيث تستطيع الأجسام المضادة أحادية النسيلة الارتباط بأهداف جزيئية محددة على الخلايا المريضة دون التأثير بشكل كبير على الخلايا السليمة.
هذا يترجم إلى “آثار جانبية أقل“ وأكثر تحملًا مقارنة بالعلاج الكيميائي الشامل، الذي قد يؤثر على الخلايا سريعة الانقسام في جميع أنحاء الجسم.
فبينما قد تحدث آثار جانبية مع العلاج الأحادي النسيلة، إلا أنها غالبًا ما تكون أقل شدة وتخصصًا.
ثانيًا، القدرة على تحقيق استجابات علاجية قوية وطويلة الأمد: في العديد من أنواع السرطان وأمراض المناعة الذاتية، أدت الأجسام المضادة أحادية النسيلة إلى سيطرة مستدامة على المرض، وبعضها يساهم في تحقيق الشفاء في حالات معينة، خاصة عندما يتم استهداف مسارات حيوية لنمو المرض.
ثالثًا، “تحسين نوعية حياة المرضى“: بفضل انخفاض الآثار الجانبية وزيادة فعالية العلاج، يمكن للمرضى الاستمرار في أنشطتهم اليومية بشكل أفضل، مما ينعكس إيجابًا على جودتها حياتهم بشكل عام.
رابعًا، “الطب الشخصي“: تتيح الأجسام المضادة أحادية النسيلة تصميم خطط علاجية تتناسب مع البصمة الجزيئية الفريدة للمرض لدى كل مريض، مما يزيد من فرص نجاح العلاج ويقلل من العلاجات غير الفعالة. هذه الفوائد مجتمعة تجعل العلاج الأحادي النسيلة محركًا رئيسيًا للتقدم في الطب الدقيق.
الآثار الجانبية للعلاج الأحادي النسيلة
على الرغم من الدقة العالية للعلاج الأحادي النسيلة، فإنه ليس خاليًا من الآثار الجانبية، والتي يمكن أن تختلف بشكل كبير اعتمادًا على نوع الجسم المضاد المستعمل والهدف الذي يستهدفه، وكذلك حالة المريض الصحية العامة.
أحد الآثار الجانبية الشائعة هو “تفاعلات التسريب (Infusion Reactions)”، والتي قد تحدث أثناء أو بعد فترة وجيزة من إعطاء الدواء.
يمكن أن تشمل هذه التفاعلات أعراضًا شبيهة بالحساسية مثل الحمى، القشعريرة، الغثيان، الطفح الجلدي، أو صعوبة التنفس. عادةً ما يتم التحكم في هذه التفاعلات بإعطاء أدوية مضادة للحساسية قبل التسريب، وبإبطاء معدل التسريب.
بالإضافة إلى ذلك، يمكن أن تحدث آثار جانبية أخرى تعتمد على آلية عمل الجسم المضاد:
- الآثار الجانبية المتعلقة بالجلد: مثل الطفح الجلدي، حب الشباب، أو جفاف الجلد، خاصة مع الأجسام المضادة التي تستهدف مستقبلات عامل نمو البشرة (EGFR).
- الآثار الجانبية المتعلقة بالجهاز الهضمي: مثل الإسهال أو الإمساك، أو الغثيان.
- الآثار الجانبية المتعلقة بالجهاز المناعي: في حالة مثبطات نقاط التفتيش المناعية، قد يؤدي تنشيط الجهاز المناعي إلى مهاجمة الأنسجة السليمة، مما يسبب التهابات في أعضاء مختلفة مثل القولون (التهاب القولون)، أو الكبد (التهاب الكبد)، أو الغدد الصماء (التهاب الغدة الدرقية).
- زيادة خطر العدوى: بعض الأجسام المضادة، خاصة تلك التي تثبط الجهاز المناعي (مثل مثبطات TNF-alpha)، يمكن أن تزيد من خطر الإصابة بالعدوى.
كلمة أخيرة
لقد أثبت العلاج الأحادي النسيلة أنه ليس مجرد دواء، بل هو نقلة نوعية في منهجية العلاج الطبي.
من خلال قدرته الفريدة على استهداف الجزيئات المحددة التي تكمن وراء الأمراض، قدم هذا النهج حلولاً علاجية دقيقة وفعالة لأمراض كانت في السابق مستعصية.
لقد حول المفاهيم البيولوجية المعقدة إلى علاجات ملموسة تُحدث فرقًا حقيقيًا في حياة المرضى حول العالم.
على الرغم من أن التحديات لا تزال قائمة، خاصة فيما يتعلق بالتكلفة وإدارة الآثار الجانبية، فإن البحث والتطوير المستمرين في هذا المجال، بدعم من المؤسسات الطبية الرائدة مثل مستشفى ليفا في تركيا، يبشر بمستقبل حيث تكون العلاجات أكثر تخصيصًا، وأكثر أمانًا.
أسئلة شائعة
هل العلاج الأحادي النسيلة هو نفسه العلاج الكيميائي أو المناعي؟
ليس تمامًا. العلاج الأحادي النسيلة هو نوع من أنواع العلاج الموجه (العلاج الذكي)، ويمكن أن يعمل أيضًا كنوع من العلاج المناعي إذا كان يستهدف نقاط التفتيش المناعية (مثل مثبطات PD-1). ولكنه يختلف عن العلاج الكيميائي الذي يستهدف الخلايا سريعة الانقسام بشكل عام.
ما هي أنواع الأمراض التي يعالجها العلاج الأحادي النسيلة؟
يعالج مجموعة واسعة من الأمراض، أبرزها العديد من أنواع السرطان (مثل سرطان الثدي، الرئة، القولون، الليمفوما، الميلانوما)؛ وأمراض المناعة الذاتية والالتهابية (مثل التهاب المفاصل الروماتويدي، الصدفية، مرض كرون، التصلب المتعدد)؛ وبعض الأمراض المعدية (مثل كوفيد-19).
هل يمكن استخدام العلاج الأحادي النسيلة لجميع مرضى السرطان؟
لا، لا يمكن استخدامه لجميع مرضى السرطان. يعتمد استخدامه على وجود “هدف جزيئي” محدد (بروتين أو طفرة) في الخلايا السرطانية لدى المريض، والذي يمكن للجسم المضاد استهدافه. يتم تحديد ذلك عبر اختبارات جينية وجزيئية على عينة الورم.
ما هي الآثار الجانبية الشائعة للعلاج الأحادي النسيلة؟
تختلف الآثار الجانبية حسب الدواء المحدد، ولكنها قد تشمل تفاعلات التسريب (مثل الحمى، القشعريرة، الطفح الجلدي)، والإرهاق، والغثيان، والإسهال. في بعض الحالات، وخاصة مع مثبطات نقاط التفتيش، قد تحدث آثار جانبية مرتبطة بالمناعة تؤثر على أعضاء مختلفة.
كم تستغرق مدة العلاج الأحادي النسيلة؟
تختلف المدة بشكل كبير بناءً على نوع المرض، ونوع الدواء، واستجابة المريض. قد يُعطى العلاج لبضعة أشهر، أو لعدة سنوات، أو حتى مدى الحياة في بعض أمراض المناعة الذاتية المزمنة. يتم تحديده من قبل الطبيب المعالج بناءً على حالة المريض.
هل العلاج الأحادي النسيلة مكلف؟
نعم، عادةً ما تكون أدوية العلاج الأحادي النسيلة باهظة الثمن نظرًا لتعقيد عملية البحث والتطوير والإنتاج البيولوجي. هذا يمثل تحديًا عالميًا في توفيرها للجميع.